Po tříletém přechodném období a 12měsíčním odkladu z důvodu pandemie SARS-CoV-2 nyní začala v Evropské unii platit nová nařízení pro zdravotnické prostředky používané u lidí. Nová a přísnější pravidla se týkají především těch, kdo zdravotnické prostředky vyrábí, dovážejí a prodávají, nicméně i stomatologičtí odborníci by měli vědět, že distributoři mají povinnost vést registr všech stížností nebo hlášení, které obdrží od zdravotníků nebo pacientů, a předávat tyto stížnosti výrobci zařízení nebo dovozci.
Nařízení Rady (EU) 2017/745, běžně označované jako „nařízení pro zdravotnické prostředky“, vešlo v platnost 25. května 2017 s tříletou odkladnou lhůtou. Toto nařízení zrušilo Směrnici Rady 93/42/EHS, známou jako „směrnice o zdravotnických prostředcích“, a Směrnici Rady 90/385/EHS, která v Evropské unii upravovala aktivní implantační zdravotnické prostředky. Spolu s tímto nařízením vešlo v platnost i další nařízení – Nařízení Rady (EU) 2017/746, známé jako nařízení pro in vitro diagnostiku – které má upravovat diagnostické zdravotnické prostředky a kterému vyprší pětileté přechodné období v květnu 2022.
Evropská komise v dubnu loňského roku oznámila 12měsíční odklad platnosti Nařízení Rady (EU) 2017/745. Komise ve svém prohlášení vysvětlila, že toto rozhodnutí učinila proto, aby mohly členské státy, zdravotnické instituce a komerční subjekty upřít veškeré síly na boj s pandemií. „Právě teď nepřipadají v úvahu zamítnutí nebo průtahy při získávání certifikátů pro klíčové zdravotnické prostředky a jejich uvedení na trh,“ komentoval situaci v tiskové zprávě Margaritis Schinas, viceprezident pro propagaci našeho evropského způsobu života.
Co se v rámci nových nařízení EU pro zdravotnické prostředky změní?
Ve srovnání se zrušenou směrnicí o zdravotnických prostředcích mění nové nařízení rozsah zdravotnických prostředků a způsob jejich klasifikace. Právní předpisy například obsahují nová pravidla pro prostředky využívající nebezpečné látky a pro softwarové aplikace. U některých prostředků upravuje nařízení klasifikaci a upravuje také některé prostředky, které byly dříve z působnosti směrnice o zdravotnických prostředcích vyňaty.
Nařízení rovněž přináší změny v dohledovém procesu. Podle nového nařízení mohou ověřovat vhodnost zdravotnických prostředků pro použití v EU pouze orgány nařízením k tomu pověřené. Podle dokumentu vydaného Evropskou obchodní právní kanceláří se sídlem v Bruselu a Evropskou asociací dentálních prodejců – který viděli i zástupci i Dental Tribune International – brání situace v oblasti veřejného zdraví v Evropě stanovit dostatek pověřených orgánů. Protože některé pověřené orgány určené původní směrnicí o zdravotnických prostředcích nemusí dostat pověření i podle nového nařízení, očekává se, že někteří výrobci zdravotnických prostředků budou muset změnit pověřené orgány.
Další příklady různých změn, které nové nařízení přineslo, zahrnují přepracovanou koncepci podnikatelského subjektu rozlišující mezi výrobcem, autorizovaným obchodním zástupcem, dovozcem a distributorem. Všechny podnikatelské subjekty musí splňovat požadavky nového nařízení a předpokládá se zvýšení odpovědnosti všech zúčastněných.
Nové nařízení také přináší zvýšený dohled po uvedení zdravotnických prostředků na trh a členské státy EU musí přijmout sankce za porušení požadavků nařízení. Na zdravotnických prostředcích musí být umístěny jedinečné identifikační štítky, aby mohly být zařazeny do nové evropské databáze. Databáze nazvaná EUDAMED bude zaznamenávat registrace jednotlivých zdravotnických prostředků, akreditovaných pověřených orgánů a rovněž certifikáty a hlášení o incidentech týkajících se bezpečnosti a klinické funkčnosti zdravotnických prostředků.
Distributoři budou povinni vést záznamy veškerých stížností nebo hlášení, které obdrží od zdravotnických odborníků a musí je neprodleně předávat výrobci a/nebo dovozci dotyčného zdravotnického prostředku. Distributoři zdravotnických prostředků musí rovněž vést registr nevyhovujících zdravotnických prostředků a i těch, které byly staženy z oběhu nebo z trhu.
Redakční poznámka: Úplné znění nového nařízení v anglickém jazyce je k dispozici online na (https://eur-lex.europa.eu/eli/reg/2017/745/oj). Článek byl publikován v mezinárodním vydání časopisu digital – international magazine of digital dentistry, Vol. 2, Issue 2/2021.
Pět let od svého zavedení zásadním způsobem mění Nařízení EU o zdravotnických prostředcích 2017/745 (Medical Device Regulation, MDR) proces ...
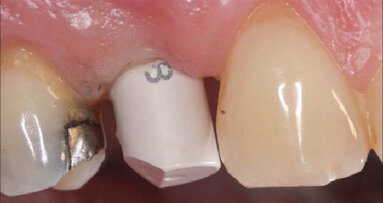
PERUGIA, Itálie: V posledních letech došlo v oblasti výroby zubních náhrad k výraznému posunu díky nástupu aditivních výrobních technologií. ...
KODAŇ/DÁNSKO: Zubní lékaři nyní mohou využívat zařízení na digitální ...
AUCKLAND, Nový Zéland: Vědci z Nového Zélandu vyvinuli ChewIt, zcela nové zařízení s individuálně konfigurovatelným rozhraním, které se nosí ...
Vláda ČR 23. března jednomyslně schválila pozastavení elektronické evidence tržeb (EET), jejíž povinnost měla pro zdravotnické profese vstoupit ...
Článek pojednává o přípravě a realizaci distanční výuky v oboru specializace Zubní technik – Fixní a snímatelné náhrady, z důvodu pandemie...
Mezinárodní dentální veletrh Pragodent již 26 let neodmyslitelně patří k podzimní dentální sezóně. Po 3 dny se zde pravidelně schází ...
LUCEMBURK: Vysoký podíl praktických zubních lékařů nezajistil zemím EU rovnoměrnou dostupnost zubní péče. Nová data Eurostatu ukazují, že v ...
Z rozsáhlého přehledu o problematice recidivy, který zahrnuje odborné studie za posledních 40 let (Bondemark et al., ...
Anatomie a příroda nás denně stále učí. Ošetření kořenových kanálků, ačkoli se ...
Živý webinář
Čt. 7 května 2026
8:30 (CET) Prague
Živý webinář
Po. 11 května 2026
6:00 (CET) Prague
Živý webinář
Po. 11 května 2026
7:00 (CET) Prague
Živý webinář
Út. 12 května 2026
7:00 (CET) Prague
Živý webinář
Čt. 14 května 2026
6:00 (CET) Prague
Živý webinář
Čt. 14 května 2026
8:00 (CET) Prague
Prof. Hani Ounsi DDS PhD FICD
Živý webinář
Út. 19 května 2026
5:00 (CET) Prague



 Rakousko / Österreich
Rakousko / Österreich
 Bosna a Hercegovina / Босна и Херцеговина
Bosna a Hercegovina / Босна и Херцеговина
 Bulharsko / България
Bulharsko / България
 Chorvatsko / Hrvatska
Chorvatsko / Hrvatska
 Česká republika & Slovensko / Česká republika & Slovensko
Česká republika & Slovensko / Česká republika & Slovensko
 Francie / France
Francie / France
 Německo / Deutschland
Německo / Deutschland
 Řecko / ΕΛΛΑΔΑ
Řecko / ΕΛΛΑΔΑ
 Maďarsko / Hungary
Maďarsko / Hungary
 Itálie / Italia
Itálie / Italia
 Nizozemsko / Nederland
Nizozemsko / Nederland
 Severské země / Nordic
Severské země / Nordic
 Polsko / Polska
Polsko / Polska
 Portugalsko / Portugal
Portugalsko / Portugal
 Rumunsko a Moldavsko / România & Moldova
Rumunsko a Moldavsko / România & Moldova
 Slovinsko / Slovenija
Slovinsko / Slovenija
 Srbsko & Černá Hora / Србија и Црна Гора
Srbsko & Černá Hora / Србија и Црна Гора
 Španělsko / España
Španělsko / España
 Švýcarsko / Schweiz
Švýcarsko / Schweiz
 Turecko / Türkiye
Turecko / Türkiye
 Velká Británie & Irsko / UK & Ireland
Velká Británie & Irsko / UK & Ireland
 International / International
International / International
 Brazílie / Brasil
Brazílie / Brasil
 Kanada / Canada
Kanada / Canada
 Latinská Amerika / Latinoamérica
Latinská Amerika / Latinoamérica
 USA / USA
USA / USA
 Čína / 中国
Čína / 中国
 Indie / भारत गणराज्य
Indie / भारत गणराज्य
 Pákistán / Pākistān
Pákistán / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Izrael / מְדִינַת יִשְׂרָאֵל
Izrael / מְדִינַת יִשְׂרָאֵל
 Alžírsko, Maroko a Tunisko / الجزائر والمغرب وتونس
Alžírsko, Maroko a Tunisko / الجزائر والمغرب وتونس
 Blízký východ / Middle East
Blízký východ / Middle East












































To post a reply please login or register